Mahasweta Pal, rédacteur médical indépendant at Kolabtree, writes about ongoing les essais cliniques to test the efficacy of convalescent plasma treatment for COVID-19.
À ce jour, le Remdesivir et le Favipiravir restent les seuls médicaments disponibles ayant un statut d'urgence approuvé par la FDA pour traiter les maladies à coronavirus, qui ne sont approuvés et accessibles que dans quelques pays (États-Unis, Italie, Chine et Japon). En outre, l'hydroxychloroquine et la chloroquine, qui étaient les médicaments les plus fréquemment utilisés contre les infections par le SRAS-COV-2, ont été associées à des effets indésirables. des problèmes graves de rythme cardiaque et une autre étude récente a conclu que, bien qu'ils soient efficaces contre les maladies auto-immunes et le paludisme, ils n'a pas pu montrer de bénéfice significatif contre l'infection à coronavirus.. Même le bras de l'essai SOLIDARITY de l'Organisation mondiale de la santé, basé sur l'hydroxychloroquine, a été interrompu.
Dans plusieurs pays, la population de patients comprend des cas asymptomatiques de COVID-19, et le besoin de traitements contre les cas légers et sévères de COVID-19 a considérablement augmenté, ce qui a conduit les grandes entreprises pharmaceutiques à envisager d'autres traitements en cours d'essai clinique, compte tenu de l'émergence de la crise mondiale.
Des études antérieures sur le traitement des infections à coronavirus telles que le SRAS, le MERS et d'autres infections de ce type ont été réalisées. les maladies virales, dont l'Ebolavirus et de la pandémie de grippe A H1N1 ont montré que perfusion de plasma de convalescence est un solution provisoire viable for treating patients with life-threatening manifestations of severe acute respiratory syndrome coronavirus 2 (SARS-COV-2) coronavirus disease. Therefore, here is a brief look at how this biological intervention is helping in the pandemic management in soins de santé systems worldwide.
Essais cliniques sur la thérapie par plasma convalescent
Dans les 96 essais en cours dans le monde, le plasma convalescent (PC) contenant des anticorps contre le SRAS-CoV-2 est en train d'être étudié en tant que traitement expérimental pour les patients atteints de COVID-19. Le traitement par PC ou immunoglobuline hyperimmune a été limité à des conceptions à un seul bras pour la plupart. Jusqu'à présent, 56200+ patients ont été recrutés dans des essais, tandis que le recrutement reste ouvert dans la plupart des centres. Le critère d'évaluation le plus courant dans chaque essai est la modification des scores SOFA (Sequential Organ Failure Assessment) mesurés 1, 3, 7 et 28 jours après l'administration de la PC au jour 0 de l'essai. Les critères d'inclusion pour les essais sur la PC sont les patients adultes gravement malades, les patients présentant des complications modérément graves, notamment une insuffisance respiratoire et/ou multisystème, et les patients présentant un tableau clinique modéré mais avec des comorbidités à long terme, notamment le diabète, l'hypertension ou des affections rhumatoïdes.
Une étude critique portant sur 10 patients gravement malades atteints de COVID-19 et provenant de 3 hôpitaux différents de Wuhan suggère que la transfusion de PC à titre élevé peut neutraliser efficacement le SRAS-CoV-2, entraînant une diminution des réponses inflammatoires et une amélioration de l'état des symptômes sans effets indésirables graves.
Early Études de phase I menée dans divers hôpitaux de Chine a conclu que l'administration de PC améliorait les symptômes respiratoires dans les 3 à 5 jours suivant la transfusion. Sur le site une autre étudeLes patients ont vu leurs scores SOFA améliorés et leur charge virale réduite après avoir reçu une PC combinée à de la méthylprednisolone, une ventilation mécanique et des agents antiviraux. Le traitement a permis de récupérer du SDRA en 12 jours, montrant ainsi l'applicabilité de la PC dans une cohorte de petits patients gravement malades atteints de COVID-19 et de SDRA.
Un procès en cours en Colombie teste l'efficacité du plasma de convalescence associé à l'hydroxychloroquine par rapport à l'hydroxychloroquine sur des patients hospitalisés atteints du COVID-19. Les chercheurs cherchent à évaluer les changements de la charge virale sur des périodes de 1, 4, 7, 14 et 28 jours, ainsi que le développement d'anticorps IgM et IgG en tant que mesures primaires et la réduction de la période d'hospitalisation et de l'admission aux soins intensifs en tant que mesure secondaire. Le NIH a également a lancé un essai clinique pour collecter le plasma de patients adultes qui se sont rétablis de la maladie. Les donneurs de plasma intéressés peuvent également consulter cette ressource nationale mise en place par les NIH et l'Agence américaine pour le développement international (USAID). Santé publique and pandemic response team dédié aux centres médicaux permettant une collecte sûre du plasma.
Directive de l'USFDA sur l'utilisation clinique expérimentale du plasma de convalescence
Le traitement ne doit être administré qu'en tant qu'intervention d'urgence par le biais d'essais cliniques, de demandes d'accès élargi (Expanded Access IND Applications) (la disposition prise par la FDA pour les patients qui n'ont pas pu être inclus dans les essais cliniques), et IND d'urgence pour un seul patient (patients COVID-19 exclus des essais mais dont le pronostic vital est sérieusement engagé) demandé par les médecins en chef de l'hôpital ou du centre médical.
L'USFDA est très stricte en ce qui concerne l'administration de PC, car ces études cliniques présentent le risque d'exposer les patients à des antigènes potentiellement immunogènes qui compliqueront les transfusions futures, et elles exposent les patients au risque de réactions transfusionnelles. En outre, l'utilisation de plasma standard comme bras de contrôle, qui comporte les mêmes risques que la PC mais aucun de ses avantages, peut masquer certains des risques de l'utilisation de la PC qui pourraient être détectés autrement.
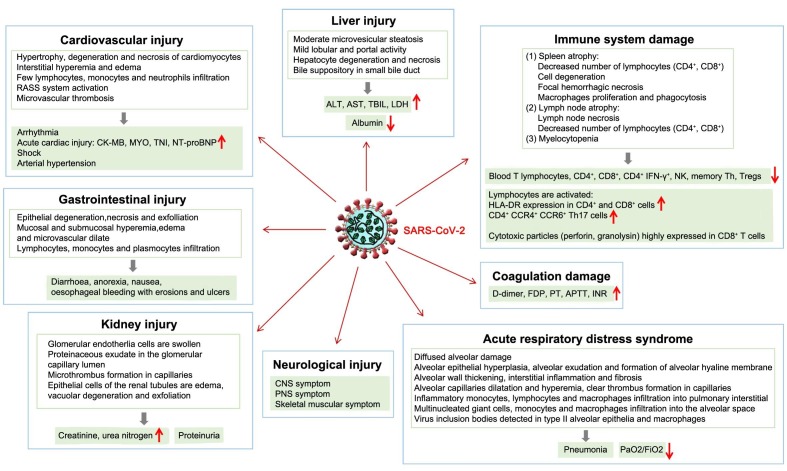
Mécanisme de la thérapie par perfusion de plasma convalescent
Composants du sang de convalescence sont dérivés du sérum ou du sang total de patients qui se sont rétablis de l'infection spécifique (dans le cas présent, COVID-19) et sont considérés comme la source d'anticorps neutralisant le SRAS-CoV-2. Historiquement, l'immunothérapie passive fait appel au sang total convalescent, au plasma convalescent, à l'immunoglobuline humaine mélangée pour une administration intraveineuse ou intramusculaire, à l'immunoglobuline humaine à haut titre et aux anticorps polyclonaux ou monoclonaux. Cependant, le plasma collecté par aphérèse est actuellement le traitement préféré. Les produits sanguins convalescents ont une longue expérience en matière de sécurité ; toutefois, ils peuvent augmenter le risque de renforcement de l'infection par les anticorps (ADE), un phénomène qui peut rendre une personne susceptible d'être infectée par d'autres virus en présence d'anticorps.
Malgré les preuves de longue date de l'utilisation de la PC ou de l'immunoglobuline hyperimmune, son efficacité clinique reste incertaine et les conclusions sont faibles, probablement parce que la PC n'a été utilisée que dans des situations critiques, lors d'épidémies/pandémies massives, nécessitant des actions immédiates. L'efficacité du traitement par PC semble varier en fonction de l'agent pathogène et des protocoles de traitement (par exemple, le moment, le volume et le dosage de l'administration).
Since this is one of the few available viable treatments under application against the 2019-nCoV, there is an impending need for governments to formulate soins de santé practice guidelines. Guidelines that ensure biosafety of collected medicinal and biological products, their storage and overall safety, and preventing contamination have yet to be set in place. Un commentaire clé de l'USFDA en collaboration avec des chercheurs d'autres COVID-19 clés souligne également la nécessité pour les pays à revenu faible et intermédiaire de veiller à maintenir un approvisionnement suffisant en composants sanguins de qualité et sûrs pour la transfusion, ce qui est essentiel pour répondre aux besoins de soins de santé primaires de la population. Les réponses à l'épidémie de COVID-19 réaffirment l'importance de la mise en place d'un système sanguin national organisé et durable, tandis que des mesures sont prises pour fournir du plasma convalescent COVID-19 collecté, testé et traité de manière appropriée pour une utilisation clinique expérimentale.
Utilisation immédiate du plasma convalescent permet une méthode prometteuse de prise en charge des patients atteints de COVID-19 pendant que des vaccins et des traitements spécifiques sont évalués et mis à l'échelle. La PC provenant de donneurs ayant guéri du COVID-19 est considérée comme la plus prometteuse lorsqu'elle est utilisée en prophylaxie ou lorsqu'elle est administrée peu de temps après l'apparition des symptômes (dans les 14 jours). L'immunité est considérée comme pouvant durer des semaines à des mois.